摘要:科學(xué)家們已經(jīng)利用細(xì)菌的潛力來幫助建造模擬現(xiàn)實生活功能的高級合成細(xì)胞。
科學(xué)家們已經(jīng)利用細(xì)菌的潛力來幫助建造模擬現(xiàn)實生活功能的高級合成細(xì)胞。
由布里斯托大學(xué)領(lǐng)導(dǎo)的這項研究今天發(fā)表在《Nature》雜志上,在部署合成細(xì)胞(又稱原型細(xì)胞)方面取得了重要進(jìn)展,可以更準(zhǔn)確地代表活細(xì)胞的復(fù)雜成分、結(jié)構(gòu)和功能。

圖1 在部署合成細(xì)胞方面的重要進(jìn)展(圖源:[1])
從自下而上的合成生物學(xué)和生物工程到生命起源研究,在原始細(xì)胞中建立真實的功能是一個跨越多個領(lǐng)域的全球性重大挑戰(zhàn)。之前用微膠囊模擬原型細(xì)胞的嘗試都失敗了,所以研究團隊轉(zhuǎn)向利用細(xì)菌,用一種活的材料組裝過程來構(gòu)建復(fù)雜的合成細(xì)胞。
布里斯托爾大學(xué)化學(xué)學(xué)院的Stephen Mann教授和馬克斯普朗克布里斯托爾原型生物中心(Bristol Centre for Protolife Research)的Can Xu、Nicolas Martin(目前在波爾多大學(xué))和Mei Li等同事展示了一種利用充滿活細(xì)菌的粘性微滴作為微觀建筑場地來構(gòu)建高度復(fù)雜的原型細(xì)胞(protocells)的方法。
在第一步中,研究小組將空液滴暴露在兩種細(xì)菌中。一個種群自發(fā)地在液滴中捕獲,而另一個種群被困在液滴表面。然后,這兩種類型的細(xì)菌都被摧毀,從而釋放出的細(xì)胞成分仍然被困在液滴內(nèi)部或表面,以產(chǎn)生含有數(shù)千個生物分子、部件和機械的膜包覆細(xì)菌原型細(xì)胞。研究人員發(fā)現(xiàn),原型細(xì)胞能夠通過糖酵解產(chǎn)生能量豐富的分子(ATP),并通過體外基因表達(dá)合成RNA和蛋白質(zhì),這表明遺傳的細(xì)菌成分在合成細(xì)胞中仍然活躍。
為了進(jìn)一步測試該技術(shù)的能力,研究小組采用了一系列化學(xué)步驟,在結(jié)構(gòu)和形態(tài)上改造細(xì)菌原型細(xì)胞。釋放出來的細(xì)菌DNA被濃縮成一個單一的核樣結(jié)構(gòu),液滴內(nèi)部滲透著細(xì)胞骨架狀的蛋白絲網(wǎng)絡(luò)和膜界的水液泡。
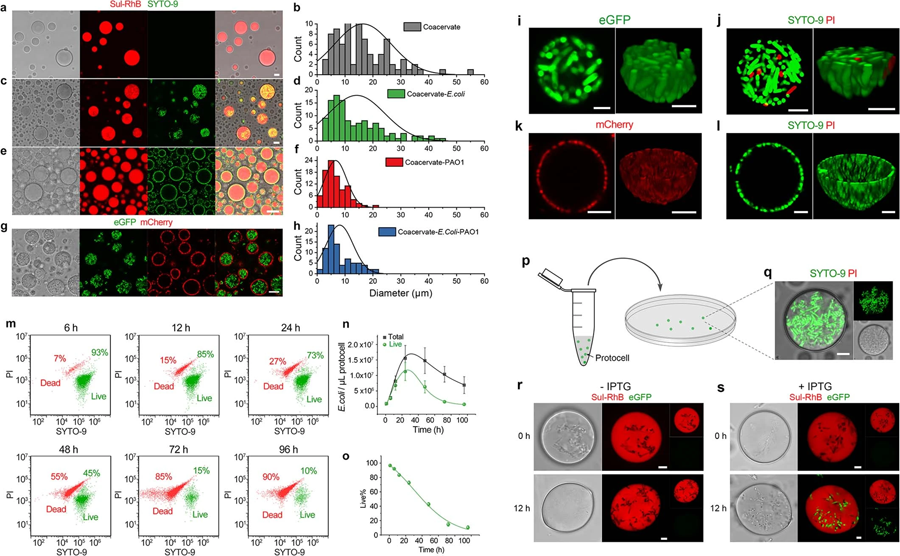
圖2 凝聚物微滴中捕獲的細(xì)菌菌落分布和存活率(圖源:[1])
作為構(gòu)建合成/活細(xì)胞實體的一步,研究人員將活細(xì)菌植入原型細(xì)胞,以產(chǎn)生自給自足的ATP生產(chǎn),并為糖酵解、基因表達(dá)和細(xì)胞骨架組裝提供長期能量。奇怪的是,由于現(xiàn)場細(xì)菌代謝和生長,原生物結(jié)構(gòu)采用了類似阿米巴的外部形態(tài),從而產(chǎn)生了具有集成生命屬性的細(xì)胞仿生系統(tǒng)。
通訊作者Stephen Mann教授說:“在合成細(xì)胞中達(dá)到高度的組織和功能復(fù)雜性是困難的,特別是在接近平衡的條件下。希望我們目前的細(xì)菌起源方法將有助于增加當(dāng)前原型細(xì)胞模型的復(fù)雜性,促進(jìn)無數(shù)生物成分的集成,并使充滿能量的模擬細(xì)胞系統(tǒng)得以發(fā)展?!?/div>
圖1 在部署合成細(xì)胞方面的重要進(jìn)展(圖源:[1])
圖2 凝聚物微滴中捕獲的細(xì)菌菌落分布和存活率(圖源:[1])
第一作者、布里斯托大學(xué)的研究助理Can Xu博士補充說:“我們的生物材料組裝方法為自下而上構(gòu)建共生生物/合成細(xì)胞結(jié)構(gòu)提供了機會。例如,利用工程細(xì)菌,應(yīng)該可以制造復(fù)雜的模塊,用于合成生物學(xué)的診斷和治療領(lǐng)域,以及一般的生物制造和生物技術(shù)?!?/div>
參考資料:
[1] Living material assembly of bacteriogenic protocells
摘要:科學(xué)家們已經(jīng)利用細(xì)菌的潛力來幫助建造模擬現(xiàn)實生活功能的高級合成細(xì)胞。
科學(xué)家們已經(jīng)利用細(xì)菌的潛力來幫助建造模擬現(xiàn)實生活功能的高級合成細(xì)胞。
由布里斯托大學(xué)領(lǐng)導(dǎo)的這項研究今天發(fā)表在《Nature》雜志上,在部署合成細(xì)胞(又稱原型細(xì)胞)方面取得了重要進(jìn)展,可以更準(zhǔn)確地代表活細(xì)胞的復(fù)雜成分、結(jié)構(gòu)和功能。

圖1 在部署合成細(xì)胞方面的重要進(jìn)展(圖源:[1])
從自下而上的合成生物學(xué)和生物工程到生命起源研究,在原始細(xì)胞中建立真實的功能是一個跨越多個領(lǐng)域的全球性重大挑戰(zhàn)。之前用微膠囊模擬原型細(xì)胞的嘗試都失敗了,所以研究團隊轉(zhuǎn)向利用細(xì)菌,用一種活的材料組裝過程來構(gòu)建復(fù)雜的合成細(xì)胞。
布里斯托爾大學(xué)化學(xué)學(xué)院的Stephen Mann教授和馬克斯普朗克布里斯托爾原型生物中心(Bristol Centre for Protolife Research)的Can Xu、Nicolas Martin(目前在波爾多大學(xué))和Mei Li等同事展示了一種利用充滿活細(xì)菌的粘性微滴作為微觀建筑場地來構(gòu)建高度復(fù)雜的原型細(xì)胞(protocells)的方法。
在第一步中,研究小組將空液滴暴露在兩種細(xì)菌中。一個種群自發(fā)地在液滴中捕獲,而另一個種群被困在液滴表面。然后,這兩種類型的細(xì)菌都被摧毀,從而釋放出的細(xì)胞成分仍然被困在液滴內(nèi)部或表面,以產(chǎn)生含有數(shù)千個生物分子、部件和機械的膜包覆細(xì)菌原型細(xì)胞。研究人員發(fā)現(xiàn),原型細(xì)胞能夠通過糖酵解產(chǎn)生能量豐富的分子(ATP),并通過體外基因表達(dá)合成RNA和蛋白質(zhì),這表明遺傳的細(xì)菌成分在合成細(xì)胞中仍然活躍。
為了進(jìn)一步測試該技術(shù)的能力,研究小組采用了一系列化學(xué)步驟,在結(jié)構(gòu)和形態(tài)上改造細(xì)菌原型細(xì)胞。釋放出來的細(xì)菌DNA被濃縮成一個單一的核樣結(jié)構(gòu),液滴內(nèi)部滲透著細(xì)胞骨架狀的蛋白絲網(wǎng)絡(luò)和膜界的水液泡。

圖2 凝聚物微滴中捕獲的細(xì)菌菌落分布和存活率(圖源:[1])
作為構(gòu)建合成/活細(xì)胞實體的一步,研究人員將活細(xì)菌植入原型細(xì)胞,以產(chǎn)生自給自足的ATP生產(chǎn),并為糖酵解、基因表達(dá)和細(xì)胞骨架組裝提供長期能量。奇怪的是,由于現(xiàn)場細(xì)菌代謝和生長,原生物結(jié)構(gòu)采用了類似阿米巴的外部形態(tài),從而產(chǎn)生了具有集成生命屬性的細(xì)胞仿生系統(tǒng)。
通訊作者Stephen Mann教授說:“在合成細(xì)胞中達(dá)到高度的組織和功能復(fù)雜性是困難的,特別是在接近平衡的條件下。希望我們目前的細(xì)菌起源方法將有助于增加當(dāng)前原型細(xì)胞模型的復(fù)雜性,促進(jìn)無數(shù)生物成分的集成,并使充滿能量的模擬細(xì)胞系統(tǒng)得以發(fā)展?!?/div>
第一作者、布里斯托大學(xué)的研究助理Can Xu博士補充說:“我們的生物材料組裝方法為自下而上構(gòu)建共生生物/合成細(xì)胞結(jié)構(gòu)提供了機會。例如,利用工程細(xì)菌,應(yīng)該可以制造復(fù)雜的模塊,用于合成生物學(xué)的診斷和治療領(lǐng)域,以及一般的生物制造和生物技術(shù)?!?/div>
參考資料:
[1] Living material assembly of bacteriogenic protocells



